Le Cancer du pancréas reste l’un des diagnostics médicaux les plus redoutés, car il progresse souvent sans signes clairs. Pourtant, un virage technologique se dessine : une techologie innovante venue de Taïwan combine analyse sanguine, spectroscopie RMN et intelligence artificielle pour viser une détection précoce bien plus fiable. L’idée intrigue autant qu’elle rassure : lire dans le sang une “empreinte” métabolique, puis laisser un algorithme repérer des patterns invisibles pour l’œil humain. Dans une étude publiée dans Nature Communications, la plateforme PanMETAI annonce des performances qui changent la conversation, avec une précision 94% dans certains scénarios, et des scores très élevés sur des cohortes à risque.
Ce qui rend l’approche fascinante, c’est son côté “hardware + data”. D’un côté, une chaîne de mesure RMN capable d’extraire des centaines de milliers de signaux biochimiques à partir d’un volume minuscule de sang. De l’autre, un modèle d’IA qui fusionne ces signaux avec quelques variables cliniques simples. À la clé, un outil qui pourrait servir de filtre non invasif avant l’imagerie. Dans un paysage 2026 où les labos automatisent, où les hôpitaux consolident leurs données, et où la santé devient un terrain majeur de l’IA appliquée, PanMETAI illustre une tendance : faire du diagnostic médical une discipline de calcul, sans perdre la rigueur clinique.
En Bref
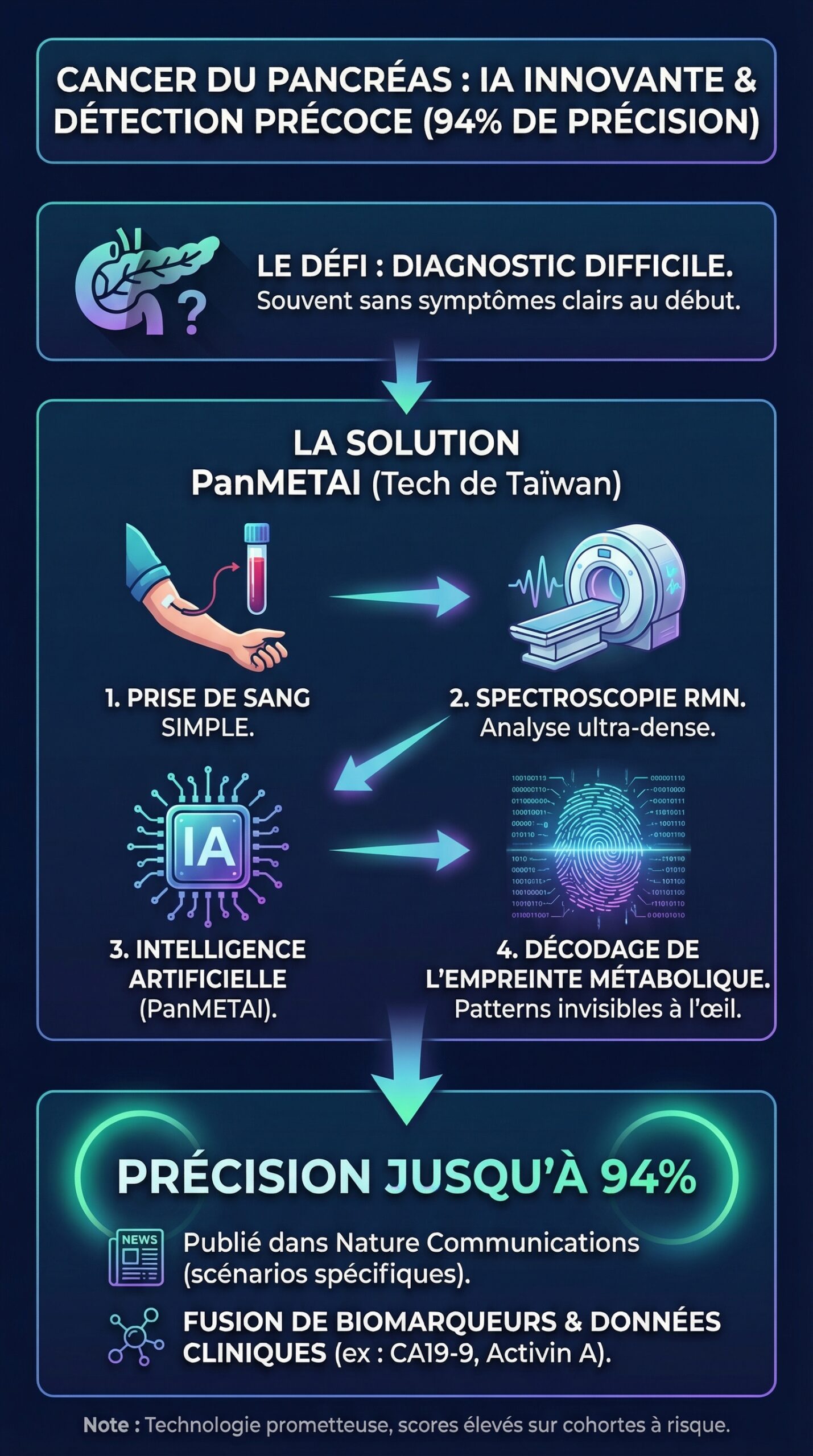
- PanMETAI associe RMN et intelligence artificielle pour une détection précoce du Cancer du pancréas via une analyse sanguine.
- L’étude rapporte jusqu’à précision 94% selon les tests, avec une sensibilité autour de 93% et une spécificité autour de 94% sur une cohorte à haut risque à Taipei.
- Le système s’appuie sur des biomarqueurs (dont CA19‑9, Activin A) et une “empreinte” métabolique massive issue d’environ 110 µL de sang.
- Une validation externe sur 322 personnes en Lituanie montre une détection d’environ 90% des cancers, tout en identifiant correctement ~83% des sujets non malades.
Cancer du pancréas et dépistage: pourquoi la détection précoce reste si difficile
Le surnom de “cancer silencieux” n’est pas un effet de style. Le Cancer du pancréas se développe dans une zone profonde de l’abdomen, et les symptômes initiaux ressemblent souvent à des troubles banals. Ainsi, fatigue, perte d’appétit ou douleurs diffuses peuvent passer sous le radar. Or, quand un signal devient enfin évident, la tumeur a déjà pris de l’avance. C’est précisément ce décalage qui pèse sur le pronostic, avec environ 13% de survie à cinq ans après diagnostic.
Pour comprendre le blocage, il faut regarder les outils classiques. D’un côté, l’imagerie (scanner, IRM, écho-endoscopie) fonctionne bien, mais elle arrive souvent trop tard, ou elle s’applique à des patients déjà suspectés. De l’autre, les marqueurs sanguins existent, mais ils ne suffisent pas seuls pour un dépistage large. Le CA19‑9 est le plus connu, cependant il manque de sensibilité et de spécificité aux stades précoces. Résultat : un taux “normal” ne rassure pas toujours, tandis qu’un taux “haut” peut venir d’autres causes.
Pourtant, la médecine moderne a appris à dépister des maladies silencieuses. Le succès des tests de sang occulte pour le côlon, ou des panels lipidiques pour le risque cardio, montre qu’un bon filtre change la trajectoire clinique. Alors, pourquoi pas ici ? La réponse tient à la biologie même du pancréas. Les tumeurs précoces peuvent être petites, hétérogènes, et biologiquement discrètes. En conséquence, un seul biomarqueur a peu de chances de tout capturer.
Dans les services, la population “à haut risque” devient donc centrale. Il s’agit notamment de personnes avec antécédents familiaux, pancréatite chronique, certaines mutations, ou un diabète récemment apparu chez un sujet plus âgé. Dans un parcours réaliste, un test sanguin fiable pourrait jouer un rôle de triage : il déclenche une imagerie ciblée, plutôt qu’un dépistage lourd pour tous. Cette logique, déjà utilisée en infectiologie ou en cardiologie, pourrait enfin s’imposer en oncologie pancréatique.
Un exemple concret aide à visualiser. Une clinique fictive, la “Polyclinique Aster”, suit 600 patients à risque modéré. Aujourd’hui, elle alterne examens et surveillance, avec une contrainte de planning en imagerie. Demain, un test sanguin IA pourrait réduire les explorations inutiles, tout en accélérant la prise en charge des profils les plus suspects. Ce basculement ne tient pas qu’au logiciel : il dépend aussi de la standardisation du prélèvement, du transport, et de l’interprétation. En somme, le diagnostic médical se joue autant dans la logistique que dans l’algorithme, et c’est l’insight qui prépare le terrain à PanMETAI.
PanMETAI: une technologie innovante mêlant RMN et intelligence artificielle pour une analyse sanguine ultra-dense
PanMETAI n’est pas un “simple test” au sens traditionnel. C’est une chaîne complète qui commence par la mesure physique, puis se termine par une décision probabiliste. D’abord, la plateforme exploite la spectroscopie par résonance magnétique nucléaire (RMN) sur un très faible volume, environ 110 microlitres de sang. Ensuite, elle convertit cette mesure en une quantité impressionnante de données, autour de 260 000 signaux métaboliques. Enfin, un algorithme apprend à distinguer des profils compatibles avec un cancer, en s’appuyant sur ces patterns.
Cette approche “omics” rappelle les workflows de laboratoire qui ont explosé avec la génomique, sauf qu’ici la matière première n’est pas l’ADN. Il s’agit d’une empreinte chimique dynamique, influencée par l’alimentation, l’inflammation, le microbiote, et bien sûr la tumeur. Cependant, au lieu de fuir cette complexité, PanMETAI en fait une ressource. Plus le signal est riche, plus l’IA a des chances de détecter une signature subtile, surtout aux stades I et II.
Fusion des biomarqueurs: CA19‑9, Activin A et données cliniques simples
Un point clé tient à la fusion entre métabolomique et clinique. Le modèle ne “regarde” pas uniquement la RMN. Il ingère aussi l’âge, le taux de CA19‑9, et le niveau d’une protéine nommée Activin A. Ce trio agit comme une rampe de lancement, car il apporte un contexte que la chimie brute ne fournit pas toujours. Ainsi, une variation métabolique n’a pas le même sens à 35 ans qu’à 72 ans, et l’algorithme peut l’intégrer.
Le modèle mentionné, TabPFN, s’inscrit dans une famille d’outils capables de traiter des tableaux de données hétérogènes. Concrètement, cela ressemble à un pipeline ML “propre” : normalisation, gestion du bruit, sélection implicite de features, puis classification. Toutefois, l’intérêt n’est pas le nom du modèle, mais sa capacité à généraliser. En 2026, ce point devient vital, car un test qui marche à Taipei mais échoue à Vilnius perd sa valeur clinique.
Un parallèle hardware: capteurs, bruit et calibration
Sur un blog orienté hardware, un détail saute aux yeux : la RMN n’est pas un gadget. La stabilité du champ magnétique, la calibration, et la gestion du bruit jouent un rôle direct sur la qualité des biomarqueurs dérivés. Par conséquent, industrialiser PanMETAI implique des procédures strictes, comme pour un banc de test audio haut de gamme. Si la mesure varie, la prédiction dérive. À l’inverse, une chaîne calibrée rend l’IA nettement plus fiable.
Dans les labos modernes, cette standardisation passe aussi par l’automatisation. Pipetage robotisé, traçabilité des lots, et contrôle qualité statistique deviennent des briques essentielles. Ainsi, PanMETAI ressemble moins à une app miracle qu’à un “stack” médico-technique. Et c’est exactement ce qui permet d’envisager la suite : mesurer mieux, puis apprendre mieux, afin de pousser la détection précoce là où la clinique seule plafonne.
Pour situer l’idée dans l’écosystème, une recherche vidéo sur les “blood test AI cancer detection metabolomics” montre à quel point le secteur bouillonne, entre start-ups et équipes hospitalo-universitaires.
Précision 94%: comment lire sensibilité, spécificité et validation externe sans se tromper
Une annonce de précision 94% attire l’attention, mais elle peut aussi tromper. En diagnostic médical, il faut séparer plusieurs métriques. La sensibilité mesure la capacité à repérer les malades. La spécificité mesure la capacité à écarter les non-malades. Or, un test “très sensible” peut générer des faux positifs, tandis qu’un test “très spécifique” peut rater des cas. Le bon compromis dépend du contexte, surtout pour une maladie rare, mais grave.
Dans un test en aveugle mené à Taipei chez des patients à haut risque, PanMETAI affiche une sensibilité autour de 93% et une spécificité autour de 94%. Autrement dit, sur 100 malades, environ 93 seraient correctement signalés, et sur 100 non-malades, environ 94 seraient correctement rassurés. C’est un niveau élevé pour un dépistage non invasif, surtout au regard des limites historiques du CA19‑9 seul.
Validation en Lituanie: l’épreuve du terrain
Ensuite vient la question de la généralisation. Une validation externe sur 322 personnes suivies en Lituanie rapporte environ 90% de cancers détectés, et environ 83% de sujets non malades correctement identifiés. Les chiffres bougent, car la population, les habitudes, et les pré-analyses changent. Pourtant, le signal reste fort : l’outil conserve une capacité de tri utile dans un autre pays, ce qui est rarement acquis d’emblée.
Pour les stades I et II, la précision globale reste proche de 92% selon les auteurs. C’est probablement le point le plus intéressant, car ce sont les stades où une prise en charge peut avoir plus d’impact. En revanche, ces résultats doivent être replacés dans un parcours. Un test positif n’est pas une condamnation. Il déclenche plutôt une imagerie, puis une confirmation histologique si nécessaire.
| Scénario évalué | Population | Indicateurs rapportés | Ce que cela implique en pratique |
|---|---|---|---|
| Test en aveugle (Taipei) | Patients à haut risque | Sensibilité ~93%, spécificité ~94% | Bon filtre avant imagerie, avec peu de cas manqués et peu d’alarmes inutiles |
| Validation externe (Lituanie) | 322 personnes suivies | ~90% cancers détectés, ~83% non-malades bien classés | Performance robuste malgré changement de contexte, mais plus de faux positifs possibles |
| Focus stades précoces | Stades I-II | Précision globale ~92% | Potentiel élevé pour la détection précoce, donc pour des options thérapeutiques plus efficaces |
Cas d’usage: triage intelligent dans une clinique
Reprenons la “Polyclinique Aster”. Si 200 patients sont classés “haut risque” chaque année, une stratégie réaliste serait de faire une analyse sanguine PanMETAI en première ligne. Ensuite, seuls les positifs ou les profils ambiguës iraient vers l’imagerie. Ainsi, la machine d’IRM gagne du temps, et les radiologues se concentrent sur les cas prioritaires. De plus, le patient vit un parcours plus fluide, car l’étape 1 est rapide et peu invasive.
Cependant, l’implémentation demande une gestion claire des seuils. Trop bas, le système alerte trop souvent. Trop haut, il rate des patients. C’est là que les comités hospitaliers interviennent, car ils calibrent selon la prévalence locale. Au fond, la précision 94% n’est pas une fin, mais un point de départ pour un protocole, et c’est l’insight qui conditionne l’impact réel sur la santé.
Du labo à l’hôpital: intégration, workflow et comparaisons avec d’autres approches IA
Transformer PanMETAI en outil clinique exige plus qu’un article scientifique. Il faut un workflow compatible avec les contraintes hospitalières : temps de rendu, contrôle qualité, cybersécurité, et responsabilité médicale. D’abord, le prélèvement doit être standardisé. Ensuite, l’acheminement vers la RMN doit limiter les variations. Enfin, le résultat doit s’intégrer au dossier patient, avec une traçabilité complète. Sans cela, même le meilleur algorithme reste une démo.
En parallèle, il faut comparer avec les autres voies IA déjà explorées pour le Cancer du pancréas. Plusieurs équipes travaillent sur l’analyse d’images de scanner, avec des performances parfois élevées, autour de 80–90% selon les protocoles. L’avantage de l’imagerie est clair : on “voit” la lésion. Cependant, l’imagerie implique du temps machine, des coûts, et parfois des contrastes. À l’inverse, une stratégie sanguine peut agir plus tôt, puis orienter vers l’image quand cela devient pertinent.
Ce que la RMN métabolomique apporte face aux modèles sur images
La RMN métabolomique capture un état fonctionnel. Elle reflète la manière dont l’organisme réagit, parfois avant qu’une masse soit visible. Ainsi, elle peut théoriquement détecter un signal précoce. En revanche, elle dépend de facteurs confondants, comme certaines inflammations. C’est pourquoi la fusion avec des données cliniques et des biomarqueurs traditionnels est stratégique. Elle “ancre” le signal dans un contexte, et réduit les erreurs.
Un autre aspect est la scalabilité. Les scanners existent déjà partout, mais ils sont saturés. Les RMN métabolomiques dédiées sont moins courantes, mais elles peuvent se centraliser en plateforme, un peu comme certains labos de biologie. D’un point de vue matériel, cela pose une question directe : vaut-il mieux multiplier des appareils de mesure, ou optimiser l’occupation de ceux déjà en place ? La réponse dépend du pays, du remboursement, et du volume de patients.
Checklist de déploiement: ce que les hôpitaux vont regarder
Pour garder les idées concrètes, voici une liste des critères qui reviennent souvent quand un établissement évalue une techologie innovante en diagnostic médical :
- Temps de traitement : délai entre prélèvement et résultat exploitable.
- Robustesse inter-sites : stabilité des performances entre deux centres.
- Contrôle qualité : détection des dérives instrumentales et des échantillons non conformes.
- Interopérabilité : intégration au LIS/DPI, export des scores, audit.
- Gouvernance clinique : seuils de décision, gestion des faux positifs, protocole d’imagerie.
- Sécurité : chiffrement, gestion des accès, conformité réglementaire.
Dans la “Polyclinique Aster”, le responsable biomédical demanderait aussi un plan de maintenance et des pièces détachées. Le DSI exigerait une architecture zéro-trust et des logs. Enfin, le chef de service voudrait une étude d’impact : combien de cancers détectés plus tôt, et combien d’examens évités. Quand ces trois visions s’alignent, l’innovation devient un produit, pas seulement une promesse. C’est l’insight qui prépare naturellement la discussion sur les tests et mesures en conditions réelles.
Pour suivre l’actualité, des conférences et chaînes spécialisées publient régulièrement des décryptages sur l’IA en dépistage sanguin et sur l’intégration hospitalière.
Tests, limites et prochaines étapes: vers des biomarqueurs multi-cancers et une santé plus proactive
Un résultat de recherche n’est pas un produit fini, et PanMETAI reste au stade de développement. Néanmoins, la trajectoire est lisible. D’abord, il faut des essais supplémentaires, idéalement multi-centriques, avec des protocoles harmonisés. Ensuite, il faut mesurer l’impact réel : nombre de diagnostics avancés dans le temps, effets sur les options de traitement, et coût global. Enfin, il faut clarifier les populations cibles, car un dépistage de masse n’a pas la même logique qu’un triage des patients à risque.
La question des faux positifs mérite aussi une lecture humaine. Un test sanguin “suspect” peut générer de l’anxiété. Pourtant, dans un parcours bien conçu, il sert à accélérer des examens qui auraient de toute façon été nécessaires. L’important devient alors la communication : expliquer que l’outil estime un risque, sans poser seul un diagnostic médical définitif. En pratique, cela implique des comptes rendus clairs, avec des fourchettes, et un plan d’action.
Pourquoi l’approche pourrait s’étendre à d’autres cancers
Les concepteurs évoquent déjà une adaptation à d’autres tumeurs, comme le foie ou le côlon. Ce n’est pas surprenant, car la logique est transposable : capturer une signature métabolique, puis entraîner un modèle à repérer des patterns. Toutefois, chaque organe a ses confusions possibles. Par exemple, le foie subit l’alcool, les hépatites, et la stéatose, ce qui brouille les signaux. Malgré cela, une stratégie multi-cancers pourrait émerger, avec des scores distincts et des protocoles de confirmation différents.
Dans un futur proche, le “panel” pourrait ressembler à une carte mère avec plusieurs ports : une même acquisition RMN, puis plusieurs têtes de lecture algorithmiques. Ainsi, une prise de sang unique pourrait alimenter divers modèles spécialisés. Cette idée s’aligne avec l’évolution des labos : centralisation, automatisation, et exploitation des données à grande échelle. Elle s’aligne aussi avec les attentes patients : faire simple, rapide, et utile.
Ce que 2026 change: données, réglementation et matériel
Le contexte 2026 apporte trois accélérateurs. D’abord, les hôpitaux ont souvent mieux structuré leurs données, ce qui facilite les validations externes. Ensuite, les régulateurs encadrent plus strictement les logiciels médicaux, ce qui impose des preuves, mais rassure sur la sécurité. Enfin, les constructeurs de matériel de laboratoire poussent des offres plus “clé en main”, avec maintenance, monitoring et calibrations semi-automatiques. Cette convergence rend crédible un déploiement progressif.
Dans la clinique fictive, un pilote sur 12 mois pourrait comparer deux parcours : suivi classique versus triage par PanMETAI, puis imagerie ciblée. On mesurerait le temps jusqu’au diagnostic, le taux d’examens lourds, et la satisfaction patient. Si les courbes s’améliorent, l’outil gagne sa place. Sinon, il retourne au labo pour itération. Au final, la meilleure innovation est celle qui survit à la réalité, et c’est l’insight qui distingue la tech spectaculaire de la tech utile en santé.
Le test PanMETAI remplace-t-il l’imagerie pour le cancer du pancréas ?
Non. L’objectif le plus plausible est de servir de filtre via une analyse sanguine chez des personnes à risque, puis d’orienter vers l’imagerie (scanner, IRM, écho-endoscopie) en cas de score positif ou douteux. Le diagnostic médical définitif repose encore sur des examens de confirmation, selon les protocoles cliniques.
Que signifie exactement une précision 94% pour ce test basé sur l’intelligence artificielle ?
Le chiffre dépend du scénario. Dans les résultats rapportés, il est cohérent avec une spécificité autour de 94% sur une cohorte à haut risque, et des performances globalement élevées. Il faut aussi lire la sensibilité (capacité à détecter les malades) et le contexte (population testée), car un algorithme peut performer différemment selon les centres.
Quels biomarqueurs et données sont combinés par PanMETAI ?
La plateforme exploite une empreinte métabolique issue de la RMN (des centaines de milliers de signaux), puis la combine avec des informations cliniques simples comme l’âge, le CA19‑9, et la protéine Activin A. Cette fusion aide l’algorithme à mieux distinguer sujets sains et patients atteints.
À qui un test de détection précoce du cancer du pancréas pourrait-il s’adresser en priorité ?
En priorité, aux personnes considérées à haut risque (antécédents familiaux, certaines prédispositions, pancréatite chronique, ou profils suivis de près par gastro-entérologie). Un déploiement en population générale demande des preuves supplémentaires, car la prévalence plus faible change la balance bénéfices/risques et le nombre de faux positifs.





